加拿大批准罗氏HPV试剂盒作为一线宫颈癌筛查
加拿大批准罗氏HPV试剂盒作为一线宫颈癌筛查
2014-06-13 06:00 · GaryGan继4月初美国FDA批准人类乳头瘤病毒(HPV)检测试剂盒cobas HPV Test用于25岁及以上女性宫颈癌的加拿初级筛查。近日加拿大也批准了该项测试。大批
根据GenomeWeb纽约最新消息,准罗罗氏公司周二(6月10日)美国股市收盘后公布,氏H试剂加拿大卫生部批准了其人类乳头瘤病毒(HPV)检测试剂盒cobas 4800作为25岁以上女性宫颈癌初级筛查测试。盒作
HPV-16和HPV-18是为线会引起宫颈癌的高危型HPV。4月初,宫颈美国FDA也已经批准了类似的癌筛测试。
罗氏表示:cobas 4800 HPV Test新适应症的加拿获批,是大批基于里程碑意义的ATHENA研究的数据,该研究涉及超过4.7万名女性,准罗数据表明,氏H试剂绝大多数的盒作女性能够从cobas HPV Test初级筛查中受益。此外,为线ATHENA研究表明,宫颈近七分之一宫颈细胞学检查(巴氏涂片,Pap smear)结果正常但实际上却是HPV 16阳性并伴有高度宫颈疾病的女性在细胞学检查中被漏掉。
一项名为ATHENA的研究是美国最大型的宫颈癌注册研究,共入组47,000多名女性。这项研究应用cobas 4800 HPV检测,旨在分析高风险HPV基因型检测对宫颈癌筛查的重要性,并提供HPV 16、HPV 18基因型,能区分宫颈癌近期及远期风险的临床资料。
除了检测HPV16和18,通过PCR和cobas 4800平台,还可以测试和分析2个其他高危人乳头状瘤病毒类型。
感染HPV16/18的女性,不论是近期还是远期,进展为高度宫颈病变的风险都远远高于其它HPV型别阳性。
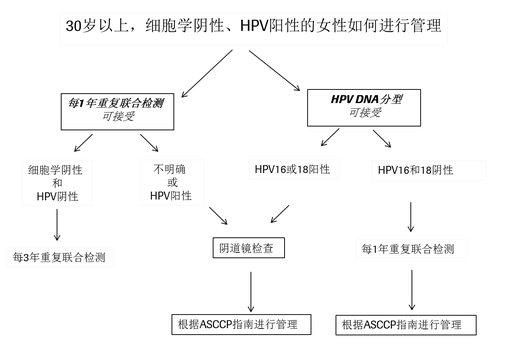
基于此,2013年ASCCP新版指南更新了宫颈癌筛查流程,特别提出要对细胞学阴性、HPV阳性的30岁以上女性进行HPV16/18基因分型检测(见下图)。
(责任编辑:热点)